Resumen
- El cáncer primario de hígado en adultos es una enfermedad por la cual se forman células malignas (cancerosas) en los tejidos del hígado.
- Hay dos tipos de cáncer primario de hígado en adultos.
- La hepatitis o la cirrosis pueden afectar el riesgo de cáncer primario de hígado en adultos.
- Entre los signos y síntomas de cáncer primario de hígado en adultos se incluyen la sensación de una masa o dolor en el costado derecho.
- Para detectar (encontrar) y diagnosticar el cáncer primario de hígado en adultos, se utilizan pruebas que examinan el hígado y la sangre.
- Ciertos factores afectan el pronóstico (probabilidad de recuperación) y las opciones de tratamiento.
El cáncer primario de hígado en adultos es una enfermedad por la cual se forman células malignas (cancerosas) en los tejidos del hígado.
El hígado es uno de los órganos más grandes del cuerpo. Tiene cuatro lóbulos y ocupa la sección superior derecha del abdomen adentro de la caja torácica.
Las siguientes son tres de las diversas funciones del hígado:
- Filtrar sustancias dañinas en la sangre para que puedan ser transportadas desde el cuerpo hasta la materia fecal y la orina.
- Producir bilis para ayudar a la digestión de las grasas de los alimentos.
- Almacenar glicógeno (azúcar) que el cuerpo usa para obtener energía.
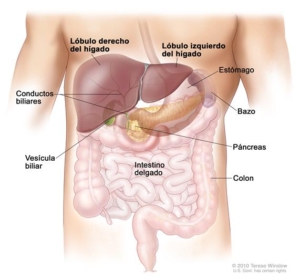
Anatomía del hígado. El hígado está en la parte superior del abdomen cerca del estómago, los intestinos, la vesícula biliar y el páncreas. El hígado tiene cuatro lóbulos. Dos lóbulos están delante del hígado y dos lóbulos pequeños (que no se muestran) están detrás del hígado.
Hay dos tipos de cáncer primario de hígado en adultos.
Carcinoma hepatocelular.
Colangiocarcinoma.
El tipo más común de cáncer primario de hígado en adultos es el carcinoma hepatocelular.
En este artículo hacemos referencia al tratamiento del cáncer primario de hígado en adultos (cáncer que comienza en el hígado). El tratamiento del cáncer que comienza en otras partes del cuerpo y se disemina al hígado no se incluye en este sumario.
El cáncer primario de hígado se puede presentar tanto en adultos como en niños. Sin embargo, el tratamiento de los niños es diferente al de los adultos.
La Hepatitis B o la Hepatitis C o la cirrosis pueden afectar el riesgo de cáncer primario de hígado en adultos.
Cualquier cosa que aumenta el riesgo de padecer de una enfermedad se llama factor de riesgo. Tener un factor de riesgo no significa que se padecerá de cáncer; no tener un factor de riesgo no significa que no se padecerá de cáncer. Consulte con su médico si piensa que puede estar en riesgo.
Los siguientes son algunos factores de riesgo del cáncer primario de hígado en adultos:
- Presentar hepatitis B o hepatitis C. El riesgo aumenta aún más si tiene ambas.
- Tener un familiar cercano con hepatitis y cáncer de hígado.
- Tener cirrosis, que puede obedecer a lo siguiente:
- Hepatitis (en particular, hepatitis C).
- Consumo por muchos años de grandes cantidades de alcohol o haber sido alcohólico durante muchos años.
- Consumir alimentos contaminados con aflatoxina (veneno de un hongo que puede crecer en alimentos, como granos y frutos secos, que no se almacenan correctamente).
- Tener hemocromatosis, una afección en la que el cuerpo absorbe y almacena más hierro de lo que necesita. El hierro adicional se almacena en el hígado, el corazón y el páncreas.
Entre los signos y síntomas de cáncer primario de hígado en adultos puede incluir dolor en el costado derecho.
Estos y otros signos y síntomas se pueden presentar por un cáncer primario de hígado en adultos u otras afecciones. Consulte con su médico si presenta cualquiera de los siguientes puntos:
- Una masa dura en el costado derecho justo debajo de la cavidad torácica.
- Malestar en la parte superior y derecha del abdomen.
- Hinchazón en el abdomen.
- Dolor cerca del omóplato derecho o en la espalda.
- Ictericia (color amarillento de la piel y la parte blanca de los ojos).
- Moretones o sangrado fáciles.
- Cansancio inusual.
- Náuseas y vómitos.
- Pérdida del apetito.
- Pérdida de peso sin razón conocida.
Para detectar (encontrar) y diagnosticar el cáncer primario de hígado en adultos, se utilizan pruebas que examinan el hígado y la sangre.
Se pueden utilizar las siguientes pruebas y procedimientos:
Examen físico y antecedentes: examen del cuerpo para verificar el estado general de salud e identificar cualquier signo de enfermedad como masas o cualquier otra cosa que parezca inusual. También se anotan datos sobre los hábitos de salud del paciente, y las enfermedades y tratamientos anteriores.
Prueba sérica de marcadores tumorales: procedimiento mediante el cual se examina una muestra de sangre para medir las cantidades de ciertas sustancias liberadas a la misma por los órganos, tejidos o células tumorales del cuerpo. Ciertas sustancias están relacionadas con tipos específicos de cáncer cuando se encuentran en concentraciones altas en la sangre. Estas se llaman marcadores tumorales. Un aumento en la concentración de alfafetoproteína (AFP) en la sangre puede ser un signo de cáncer de hígado. Otros cánceres y ciertas afecciones no cancerosas, como la cirrosis y la hepatitis, también pueden aumentar las concentraciones de AFP. Algunas veces, las concentraciones de AFP son normales, incluso cuando hay cáncer de hígado.
Pruebas de la función hepática: procedimiento para el que se analiza una muestra de sangre para medir las cantidades de ciertas sustancias liberadas por el hígado en la sangre. Una cantidad más alta que la normal de una sustancia puede ser un signo de cáncer de hígado.
Exploración por TC (exploración por TAC): procedimiento mediante el cual se toma una serie de imágenes detalladas de áreas internas del cuerpo, como el abdomen, desde ángulos diferentes. Las imágenes son creadas por una computadora conectada a una máquina de rayos X. Se puede inyectar o dar de beber un tinte para ayudar a que los órganos o los tejidos se destaquen más claramente. Este procedimiento también se llama tomografía computada, tomografía computadorizada o tomografía axial computarizada. Una exploración por TC en espiral o una TC helicoidal permiten obtener una serie de imágenes muy detalladas de áreas del interior del cuerpo mediante una máquina de rayos X que explora el cuerpo en un camino en espiral.
IRM (imágenes por resonancia magnética): procedimiento para el que se utiliza un imán, ondas de radio y una computadora para crear imágenes detalladas de áreas internas del cuerpo, como el hígado. Este procedimiento también se llama imágenes por resonancia magnética nuclear (IRMN). Para crear imágenes detalladas de los vasos sanguíneos del hígado o cercanos al hígado, se inyecta un tinte en una vena. Este procedimiento se llama ARM (angiografía por resonancia magnética).
Ecografía: procedimiento por el cual se rebotan ondas sonoras de alta energía en tejidos u órganos internos y se crean ecos. Los ecos forman una imagen de los tejidos corporales que se llama ecograma. La imagen se puede imprimir y observar más tarde.
Biopsia: extracción de células o tejidos para que un patólogo los observe al microscopio y determine la presencia de signos de cáncer. Los siguientes son los procedimientos que se usan para recoger muestras de células o tejidos:
Biopsia por aspiración con aguja fina: extracción de células, tejido o líquido mediante una aguja fina.
Biopsia central con aguja: extracción de células o tejido mediante una aguja ligeramente más ancha.
Laparoscopia: procedimiento quirúrgico para observar los órganos en el interior del abdomen a fin de determinar si hay signos de enfermedad. Se realizan pequeñas incisiones (cortes) en la pared del abdomen y se introduce un laparoscopio (un tubo delgado con luz) en una de las incisiones. Se introduce otro instrumento en la misma o en otra incisión para extraer las muestras de tejido.
No siempre es necesaria una biopsia para diagnosticar cáncer primario de hígado en adultos.
Ciertos factores afectan el pronóstico (probabilidad de recuperación) y las opciones de tratamiento.
El pronóstico (probabilidad de recuperación) y las opciones de tratamiento dependen de los siguientes aspectos:
El estadio del cáncer (el tamaño del tumor, si afecta al hígado de manera total o parcial, o si se diseminó hacia otros lugares en el cuerpo).
El funcionamiento del hígado.
La salud general del paciente, incluso si hay cirrosis del hígado.
Tratamiento del cáncer de hígado
El cáncer de hígado puede afrontarse desde diversos tratamientos, que dependerán del estado del paciente y del tumor. La resección quirúrgica, junto con el trasplante y la ablación son las únicas que ofrecen posibilidades de curación:
Resección quirúrgica
Dado que en la mayoría de los pacientes hay una cirrosis de base, hay que establecer de manera muy estricta los criterios de selección, para evitar una insuficiencia hepática posterior. Los mejores candidatos para una resección quirúrgica son los que tienen tumores únicos, están asintomáticos y tienen una función hepática conservada. En estos casos se pueden conseguir tasas de supervivencia a los 5 años del 70%. Los factores predictores de recurrencia son la invasión vascular, presencia de lesiones satélites, bajo grado de diferenciación, el tamaño del tumor, el nivel de AFP y los márgenes de resección positivos.
Trasplante de hígado
Esta es la mejor opción, ya que extirpa la lesión y además cura la enfermedad hepática preneoplásica que hubiera. Los mejores candidatos para un trasplante son aquellos con tumores de menos de 5 cm o con dos o tres tumores menores de 3 cm. Si el paciente cumple con una de esas dos condiciones, que se han denominado los criterios de Milán, se establece que el paciente puede ser seleccionado para trasplante, pues se obtiene una supervivencia similar a los pacientes sin cáncer hepático.
El mayor problema es la escasa oferta de este recurso, ya que los pacientes fallecen o progresan mientras están en la lista de espera (de donante muerto). Para intentar evitar la pérdida de pacientes en la lista de espera se han propuesto nuevos sistemas de clasificación para asignar enfermos a dicha lista, como el MELD (Model of End-staged Liver Disease), se trata de un modelo matemático de predicción de vida de un paciente con cáncer hepático basado en bilirrubina, pruebas de coagulación y función del riñón. Es más objetivo que la clasificación de Child-Pugh, va de 6 a 40 y los pacientes con mayor puntuación tienen mayor prioridad de recibir el transplante.
Otra opción razonable es el donante vivo, en la que se ha demostrado un beneficio en los análisis costo-efectividad cuando el tiempo de espera es mayor de siete meses. La morbi-mortalidad del donante ronda el 0,3-0,5%. En este caso, los criterios "oficiales" de trasplante (criterios de Milán) no tienen por qué mantenerse. En este sentido se han hecho varios estudio para poder ampliar estos criterios, siempre y cuando se mantengan las mismas supervivencias. Se ha establecido un nuevo criterio que se denomina "up to seven" siendo el nº 7 el resultado de la suma de los nódulos tumorales y el tamaño de los mismos. Con este sistema se podría ofertar el trasplante a mayor número de pacientes.
Ablación
Se trata de aplicar energía térmica (calor) por radiofrecuencia mediante un electrodo directamente sobre la lesión. Se recomiendan para lesiones menores de 3 cm (aunque sean múltiples), siempre que estén en el interior del parénquima y alejadas del hilio hepático (entrada del hígado), de grandes vasos (porta, vena o arteria hepática) o de otras estructuras próximas como estómago, colon o vesícula biliar, por el mayor riesgo de perforación de estas estructuras debido al calor. Tiene respuestas muy buenas (tasa de recurrencias del 5-20%) y con excelente tolerancia por parte del paciente. Los efectos secundarios graves no son frecuentes, pero pueden consistir en fallo hepático, trombosis venosa portal, absceso hepático, derrame pleural, quemaduras cutáneas" y se ha descrito un síndrome post-ablación que es autolimitado y consiste en síntomas gripales y elevación de transaminasas.
La radiofrecuencia ha sustituido otras técnicas de ablación como la aplicación de frío (crioablación) o la inyección de alcohol (etanol), ya que ha demostrado su superioridad en todos los estudio comparativos. Se puede hacer por vía percutánea (a través de la piel) o laparoscópica mediante control radiológico (ecografía).
Quimioembolización
Teniendo en cuenta que la mayor parte del aporte sanguíneo del hígado proviene de la arteria hepática, se han desarrollado distintas técnicas para privar de dicho aporte a las zonas donde está el tumor ocluyendo la arteria de ese territorio; esto es la embolización. Se puede hacer con partículas (incluso alcohol-etanol-) o con quimioterapia (TACE: TransArterial ChemoEmbolization). La técnica consiste en canalizar la arteria hepática y allí soltar la quimioterapia acompañada (o no) de sustancias que retienen más tiempo la quimioterapia en la zona donde se ha liberado y que son procoagulantes, es decir, favorecen la formación de un trombo (coágulo) en la arteria hepática. El efecto adverso más común es el síndrome postembolización (similar al síndrome postablación) y menos frecuentes son la colecistitis isquémica, el hipotiroidismo o el derrame pleural.
Las tasas de respuesta son del 50% y algunosbeneficios sobre la supervivencia.
En general se recomienda en pacientes sintomáticos, con hepatocarcinomas no resecables en los que el tumor es demasiado grande para la radiofrecuencia.
Tratamiento médico
En el cáncer hepático ningún tratamiento médico es curativo. Clásicamente se ha considerado un tumor quimioresistente por la existencia de múltiples genes responsables del desarrollo de resistencias a fármacos; además la hepatopatía de base que presentan la mayoría de los pacientes, condiciona la tolerancia a gran parte de los fármacos empleados. Los tratamientos médicos disponibles son los siguientes:
Terapias moleculares
El mejor conocimiento de las vías moleculares y de señalización celular en el origen de los tumores (carcinogénesis) ha hecho posible el desarrollo de gran cantidad de moléculas que resultan eficaces en el tratamiento de distintos tumores. Es lo que conocemos como terapias diana (y oncología traslacional).
Fruto de esta disciplina han aparecido fármacos de administración oral como sorafenib alcanzando estabilizaciones hasta en un 40% de casos, con supervivencias medianas de 9,2 meses, con impacto en la supervivencia global y con muy poca toxicidad. Contamos con otros fármacos llamados diana como sunitinib, bevacuzumab, etcétera, con tasas de respuesta que rondan el 18% y con medianas de supervivencia de 15 meses solos o en esquemas de combinación con la quimioterapia clásica.
Texto adaptado por HCV Sin Fronteras - 2014
Esta página web tiene un carácter meramente orientativo y, en ningún caso, se ofrece con fines diagnósticos, preventivos, terapéuticos, rehabilitadores o de investigación la información ofrecida no reemplaza, en modo alguno, a la consulta de su médico general o especialista, ni debe ser considerada como completa, inequívoca o suficiente para establecer un diagnóstico o prescripción para iniciar ningún tipo de tratamiento médico o para seguir un patrón de comportamiento
Fuentes: Instituto Nacional del Cáncer EEUU -
Cáncer de hígado Escrito por Dr. Juan José Tafalla García, oncólogo Revisado por Dr. Pablo Rivas, especialista en medicina interna - webconsultas.com