Se presentan los resultados preliminares a 24 semanas de un ensayo que evalúa este nuevo inhibidor de la proteasa contra el VHC en combinación con la terapia estándar
Boceprevir (Victrelis®) es un nuevo antiviral de acción directa contra el virus de la hepatitis C (VHC) cuya comercialización fue aprobada recientemente por Europa (véase La Noticia del Día 22/07/11). El fármaco está indicado para ser administrado por vía oral -en tres tomas diarias con comida- en combinación con la terapia estándar contra la hepatitis C (basada en interferón pegilado y ribavirina) en personas monoinfectadas con genotipo 1 del VHC, el considerado "difícil de tratar", tanto en aquellas sin experiencia en tratamientos como en las que fracasó una terapia previa.
Aunque determinadas personas coinfectadas por VIH y VHC pueden beneficiarse ya en Europa (incluida España) de un acceso precoz al fármaco si cumplen con los criterios de inclusión a un programa de uso compasivo, lo cierto es que los ensayos clínicos que evalúan el uso de este nuevo fármaco en esta población de pacientes siguen su desarrollo. La información que aportarán estos estudios es de gran importancia pues permitirá conocer al detalle la seguridad y la eficacia de boceprevir en la población coinfectada, caracterizando, entre otros aspectos, las potenciales interacciones entre dicho antiviral y los fármacos antirretrovirales (además de otros fármacos de uso habitual en personas con VIH), y otros temas relativos a su perfil de seguridad.
En este sentido, la compañía farmacéutica Merck (MSD fuera de EE UU y Canadá) acaba de anunciar a través de un comunicado de prensa los resultados preliminares a 24 semanas de su estudio de fase IIb con boceprevir en personas coinfectadas por VIH y VHC. Los resultados de dicho análisis fueron presentados en el marco del 49 Encuentro Anual de la Sociedad Americana de Enfermedades Infecciosas (IDSA, en sus siglas en inglés), celebrado en Boston (EE UU) la semana pasada.
El estudio, que cuenta con la participación de 100 personas, está evaluando el uso de boceprevir junto a la terapia estándar contra el VHC, durante un período de tiempo de 48 semanas repartidas en dos partes: cuatro semanas de tratamiento de inducción sólo con la terapia estándar, seguidas de 44 semanas en las que boceprevir se añade a interferón pegilado y ribavirina. Transcurridas las 44 semanas se interrumpe la toma de toda la terapia y se realiza un seguimiento de los pacientes hasta la semana 72, momento en el que se valorará respuesta virológica sostenida (RVS), o lo que es lo mismo la curación de la hepatitis C.
Se consideraron criterios de inclusión presentar coinfección por VIH y VHC de genotipo 1; encontrarse bajo tratamiento antirretroviral; tener unos recuentos de CD4 de, como mínimo, 200 células/mm3 y carga viral del VIH indetectable.
Los participantes fueron estratificados en función de si habían desarrollado o no cirrosis y del nivel de carga viral del VHC basal (< 800.000 UI/ml frente a ≥ 800.000 UI/ml). La mayoría de los pacientes eran no cirróticos (95%), blancos (82%) y varones (69%), con una edad media de cerca de 43 años. La mayoría de los pacientes presentaban una viremia basal del VHC elevada (88%) e infección por el VHC de genotipo 1a (65%).
Por lo que respecta a la pauta antirretroviral, se excluyó el uso de ciertos fármacos como consecuencia de las potenciales interacciones como por ejemplo los inhibidores de la transcriptasa inversa no análogos de nucleósido (ITINN), es decir nevirapina (Viramune®), etravirina (Intelence®) y efavirenz (Sustiva®; también en Atripla®); y de la clase de los inhibidores de la transcriptasa inversa análogos de nucleósido (ITIN), zidovudina (AZT, Retrovir®), estavudina (Zerit®) o didanosina (ddI, Videx®). Los participantes no debían tener experiencia en tratamientos contra la hepatitis C. En el estudio, boceprevir se administra en su dosis habitual (800mg, tres veces al día).
En la imagen se puede apreciar de forma gráfica el diseño de este estudio.
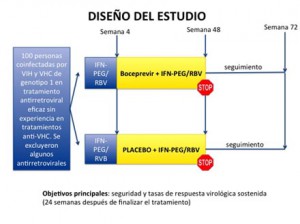 Un total de 100 participantes fueron distribuidos aleatoriamente en proporción 2:1 en los grupos con boceprevir o placebo, respectivamente. Dos pacientes del grupo de boceprevir en combinación con la terapia estándar no recibieron el fármaco experimental. Así, el análisis provisional se basó en 98 pacientes que recibieron al menos una dosis del fármaco del estudio: 64 pacientes en el grupo de boceprevir en combinación con interferón pegilado y ribavirina, y 34 pacientes en el grupo de placebo y terapia estándar.
Un total de 100 participantes fueron distribuidos aleatoriamente en proporción 2:1 en los grupos con boceprevir o placebo, respectivamente. Dos pacientes del grupo de boceprevir en combinación con la terapia estándar no recibieron el fármaco experimental. Así, el análisis provisional se basó en 98 pacientes que recibieron al menos una dosis del fármaco del estudio: 64 pacientes en el grupo de boceprevir en combinación con interferón pegilado y ribavirina, y 34 pacientes en el grupo de placebo y terapia estándar.
En los pacientes que tuvieron carga viral del VHC detectable y un descenso inferior a 2 log en el ARN de VHC a la semana 12, o viremia del VHC detectable a la semana 24, se consideró que el tratamiento había fracasado y, por lo tanto, se les interrumpió la toma de todo el régimen.
Los resultados que muestran las tasas de personas con carga viral del VHC indetectable en diferentes momentos durante las primeras 24 semanas del estudio, se resumen en la siguiente tabla:
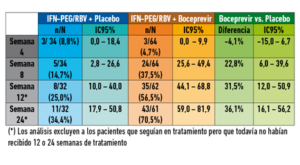 Los datos muestran cómo tras añadir boceprevir al tratamiento estándar después de las cuatro primeras semanas, los porcentajes de personas con carga viral del VHC indetectable del grupo que recibe boceprevir duplican a los observados en el grupo al que se administra terapia estándar y placebo en los diferentes puntos de medición. Así, en la semana 24 del tratamiento, el 70,5% (n=43/61) de los pacientes que recibieron boceprevir en combinación con interferón pegilado y ribavirina presentaban viremia del VHC indetectable en comparación con el 34,4% (n=11/32) de los pacientes a los que se administró un placebo junto con la terapia estándar, lo que supone una diferencia de tratamiento del 36,1%.
Los datos muestran cómo tras añadir boceprevir al tratamiento estándar después de las cuatro primeras semanas, los porcentajes de personas con carga viral del VHC indetectable del grupo que recibe boceprevir duplican a los observados en el grupo al que se administra terapia estándar y placebo en los diferentes puntos de medición. Así, en la semana 24 del tratamiento, el 70,5% (n=43/61) de los pacientes que recibieron boceprevir en combinación con interferón pegilado y ribavirina presentaban viremia del VHC indetectable en comparación con el 34,4% (n=11/32) de los pacientes a los que se administró un placebo junto con la terapia estándar, lo que supone una diferencia de tratamiento del 36,1%.
El perfil de eventos adversos en el presente análisis fue similar al observado en previos estudios llevados a cabo en personas monoinfectadas por VHC. Los más comunes , con una diferencia igual o mayor al 10% para el grupo de tratamiento que recibió boceprevir más interferón pegilado y ribavirina en comparación con el grupo al que se administró placebo y la terapia estándar control, respectivamente, fueron: neutropenia (13% frente al 3%), disgeusia [mal sabor] (25% frente al 15%), vómitos (25% frente al 15%), pirexia [ardor de estomago] (34% frente al 21%), cefaleas (28% frente al 12%) y pérdida de apetito (30% frente al 18%) [mediana de días en estudio, 211 frente a 166, respectivamente].
Se produjeron efectos secundarios clínicos graves en el 8% y el 21% de los pacientes en los dos grupos de tratamiento, respectivamente. Se produjo modificación de la dosis de cualquiera de los fármacos del estudio a causa de un acontecimiento adverso clínico en un 19% y un 21% de los pacientes, respectivamente, y un 14% y un 9% de los pacientes, respectivamente, interrumpieron el estudio a causa de un acontecimiento adverso.
Estos resultados preliminares, aunque prometedores, necesitarán confirmarse todavía con los que se obtengan del análisis a la semana 48 (respuesta al fin del tratamiento) y a la semana 72 (respuesta virológica sostenida). Sólo entonces podremos conocer bien la tasa de eficacia y el perfil de seguridad de la combinación de boceprevir y la terapia estándar en personas coinfectadas. Con todo, los hallazgos ponen de manifiesto los beneficios que este nuevo tratamiento podrían proporcionar a las personas coinfectadas por VIH y VHC de genotipo 1, el mayoritario en España.
El Ministerio de Sanidad aprobó recientemente la autorización de comercialización de boceprevir, lo que significa que el fármaco debería estar disponible a partir de ahora en todos los centros hospitalarios para todos los pacientes monoinfectados por hepatitis C que cumplan con los criterios de indicación de uso. Mientras tanto, continúa abierto en nuestro país el programa de uso compasivo de boceprevir, lo que permitirá que ciertos pacientes en determinadas circunstancias clínicas (como por ejemplo las personas coinfectadas por VIH y VHC con hepatopatía avanzada) puedan beneficiarse de forma temprana de este fármaco.
Si estás coinfectado por VIH y VHC y crees que, por el estado de tu salud hepática, podrías ser un candidato a recibir boceprevir o telaprevir (Incivo®), sería conveniente que hablaras con tu médico sobre ello, valorando y analizando los pros y los contras de acceder de forma precoz a los dos primeros antivirales orales contra el virus de la hepatitis C.
Por Juanse Hernández y Francesc Martínez - 24/10/2011 - Fuente: Elaboración propia. - Reproducido por Hepatitis 2000 bajo Copyleft de GTT-VIH
Referencia: Comunicado de prensa de Merck 20/10/2011: Interim Phase IIb Data for Merck's VICTRELISâ„¢ (boceprevir) in Patients Coinfected with Chronic Hepatitis C and HIV-1 Presented at the Infectious Diseases Society of America (IDSA) 2011 Annual Meeting.
Sulkowski M et al. Boceprevir plus peginterferon/ribavirin for the treatment of HCV/HIV co-infected patients: Interim On-Treatment Results. LB-37, Oral Abstract Session: Late Breaker Oral Abstracts. Presentado en IDSA 2011 Annual meeting, 20-23 Octubre, Boston (USA).






